동향분석
Home > 뉴스브리핑센터 > 동향분석| [KOFST 동향] 코로나바이러스감염증-19 (COVID-19)의 배경, 예방수칙 및 치료제 개발 현황 |
|
COVID-19의 배경, 예방수칙 및 치료제 개발 현황 2020.03.01 1. 코로나바이러스감염증-19(COVID-19) 배경 가. 배경 •박쥐 코로나 바이러스에서 유래한 것이 의심이 되는 이 바이러스는 Rhinolophus bat에서 유래한 바이러스와 가장 근접한 유사성 (>96%)을 가졌음 [1,2] •우한 코로나, 신종 코로나 등 다양한 명칭으로 불리던 이번 신종 코로나 변이종의 공식 명명은 세계보건기구(WHO)에 의해서 'COVID-19'로 결정되었는데 COVID-19의 'CO'는 코로나, 'VI'는 바이러스, 'D'는 질병, 19는 발병 시기인 2019년을 뜻함. 이에 국내 정부에서는 “영어식 이름(COVID-19; 씨오브이아이디-일구)이 길어 질병관리본부의 의견을 수용해 ‘코로나19(코로나일구)’라는 한글 표현을 별도로 정해 명명하기로 했음. COVID-19처럼 연도를 나타내는 이름이 붙었다는 것은 향후에도 주기적으로 이런 바이러스의 유행이 일어날 것이라는 뜻함. 나. 바이러스학 •코로나 바이러스는 숙주의 세포막에서 기원하는 인지질 껍데기를 가지고 있는데, 이 인지질의 변이가 유행이 빈번한 호흡기 감염을 유발함. •인지질 껍질에 호흡기 점액질에 친화성을 가지는 spike 프로틴이 촘촘하게 박혀 있는데 이 형태를 전자현미경으로 관찰 시 왕관(크라운) 형태의 모양을 닮았다고 해서 코로나 바이러스라는 이름이 붙었음 [3].
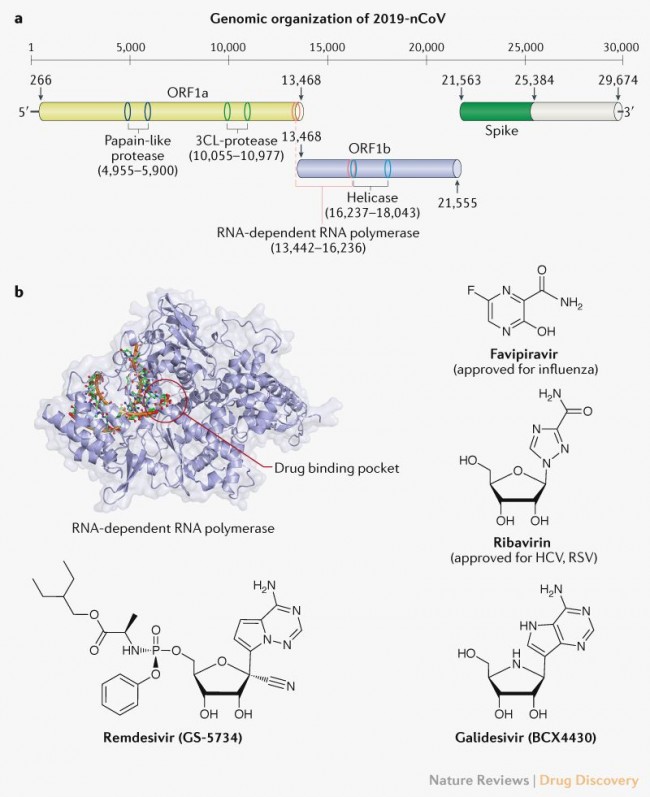
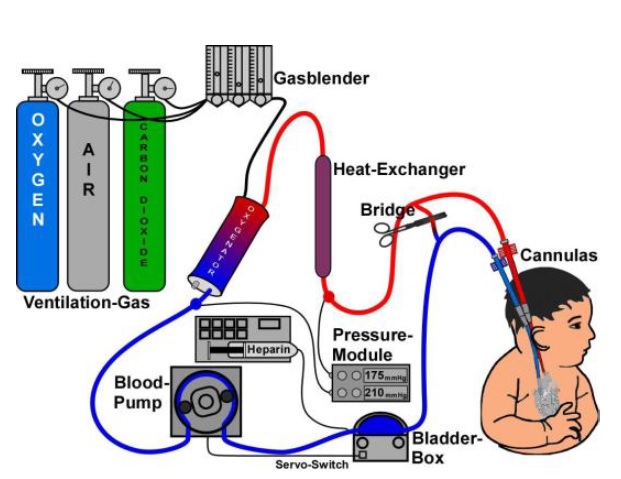
[그림 1] 코로나 바이러스의 유전체 구성정리(GenBank ID: MN908947.3)로 약물타켓으로 가능한 프로틴 구성 코딩 구획을 나타내는 그림 [4] •COVID-19는 스파이크 프로틴을 통해 ACE2(angiotensin-converting enzyme 2)를 수용체로 사용하여 숙주세포로 들어감. 스파이크 프로틴의 수용체 결합 및 막 융합은 백신 및 항바이러스제의 이상적인 타겟으로 여겨지며 특히 RNA 의존형 RNA 중합효소와 코로나바이러스의 주요 프로테아제 (3CLpro)은 SARS-COV와 매우 유사한 상동을 가지고 있고 중요 약물의 표적으로 여겨짐 [5]. •RNA 수준의 게놈은 SARS-CoV와 82% 일치하고, RdRp(RNA-dependent RNA polymerase)는 96% 일치함. RdRp를 타겟으로 항바이러스 활성을 보인 것은 음이온 중합체인 ATA(aurintricarboxylic acid), 뉴클레오시드 아날로그인 ribavirin, remdesivir이 있음. 특히 remdesivir는 저항성 돌연변이를 약화시켰음. •3CLpro(3-chymotrypsin-like protease)와 PLpro(papain-like protease)는 RNA 번역에 사용되는 효소로, 3CLpro와 PLpro에서 각각 SARS-CoV와 96%, 83%의 일치를 보였음. 현재 SARS-CoV와의 게놈 유사성을 기반으로 치료제 사용 및 연구 가능성을 검토하고 있음. 다. 임상 특징 •전파경로 – 코로나19의 사람간 전파는 큰 크기와 스파이크의 특징 때문에 비말(호흡기 분비물)을 통한 전파로 추정되고 가족간, 의료기관 내 2차감염이 보고되고 있음. 코로나19의 경우는 인지질의 스파이크에 변이가 일어나고 점액 친화력이 이전 코로나에 비해 50배 정도 강해 소량의 바이러스가 점액과 접촉해도 인후두의 호흡기 상피세포에서 초기부터 증식이 활발하게 일어남. 따라서 비교적 감염 초기부터 다른 사람에게 전파할 가능성이 큼. •잠복기 - 코로나19의 잠복기는 노출 이후 14일 이내로 예상되며, 대부분의 경우 노출 후 약 5일 이내에 감염이 발생함. 가족 클러스터 내에서의 감염은 노출 이후 대략 3-6일에 발생함. 유사한 결과로, 코로나19 폐렴으로 확진 받은 10명의 환자 분석에서 추정된 평균 잠복기는 5일이였음. •임상증상 - 코로나19 바이러스에 의한 감염도 호흡기 상피세포 감염을 통해 증상이 시작되므로 다른 독감 특히 인플루엔자 감염과 감별할수 있는 차별적인 임상적 특징은 없음. 지난 2월 14일 중국 질병통제예방센터(CDC)에서 발표한 44,672명의 확진자 역학조사에 따르면 COVID-19 (코로나 바이러스폐렴)의 증상으로 발열, 마른 기침, 피로, 코막힘, 인후통, 호흡곤란, 근육통 등이 확인되었음. •치사율 - 코로나19의 경우 아직 전파가 진행 중이라 정확한 역학 통계를 내기는 어렵지만 우리나라의 자료를 보면 치사율은 대략 1% 이하가 될 것으로 보이며, 통제가 잘되는 경우는 0.5% 이하가 될 것으로 예측됨. 소아에게 성인의 경우보다 증상들이 가볍게 나타남. H1N1(조류인플루엔자)과는 다르게 임산부들이 고위험군으로 나타나지 않음. “고령” 환자에서 질병의 중증도와 연관성을 보였으며, 80세 이상에서 14.8%의 치사율을 보임. •사망자의 사인으로 호흡부전과 쇼크 및 복합장기부전(multiple organ failure)이 확인되었음 [6]. 라. 참고할만한 공식 코로나19 사이트 · 보건복지부 코로나바이러스감염증-19(COVID-19) 사이트 http://ncov.mohw.go.kr/index_main.jsp · WHO Coronavirus disease (COVID-19) 사이트 https://www.who.int/emergencies/diseases/novel-coronavirus-2019 2. 예방수칙 가. 코로나19 예방수칙에 관한 대응지침 [7] (보건복지부 및 질병관리본부 권고, 2020.02.20 기준) •국민행동수칙 1) 물과 비누로 꼼꼼히 자주 손씻기 2) 씻지 않은 손으로 눈, 코, 입 만지지 않기 3) 기침할 때는 옷소매로 입과 코를 가리고 하기 4) 발열, 기침 등 호흡기 증상이 있는 사람과 접촉 피하기 5) 사람 많은 곳 방문 자제하기 6) 특히 노인, 임산부, 만성질환자 등은 외출 시 마스크 착용하기 •비고: 이번 코로나19에 의한 감염은 감염력이 높은 비말을 통한 감염이기 때문에 마스크 사용뿐만 아니라 손을 통한 분비물의 접촉을 최소화 하는것이 중요함. 따라서 손으로 눈, 얼굴을 만지지 않는 습관과 손을 꼼꼼히 자주 씻어주는 것이 중요함. (이때 코로나바이러스는 인지질 껍데기를 가진 바이러스이므로 특별한 손 소독제를 사용하지 않아도 계면 활성제인 비누만으로도 충분히 효과적임.) 서로 마주보고 이야기 하며 식사하거나 회식을 하는 것도 자제 하는 것이 좋음. •발열, 기침 등 호흡기 증상이 있을 시 행동수칙 1) 발열, 기침 등 호흡기 증상이 있을 시 마스크 착용하기 2) 외출을 자제하고 집에서 하루 이틀 경과를 관찰하며 휴식을 취하기 3) 의료기관 방문 시 반드시 마스크 착용 및 자차 이용 권고 4) 진료 전 의료진에게 해외 여행력 및 호흡기 질환자 접촉 여부 알리기 5) 의료인과 방역당국의 권고 잘 따르기 6) 경미한 발열, 기침 등 호흡기 증상 있을 시 대형병원, 응급실 방문 자제하고, 관할 보건소 120콜센터 또는 1339 콜센터에 먼저 상담하기 나. 코로나19 예방을 위한 마스크 사용 권고사항 [8] (보건복지부 및 질병관리본부 권고, 2020.02.20 기준) •목적 세계보건기구(WHO) 권고사항을 채택하여, 코로나19 확산을 막기 위해 공공장소에서 사용하는 마스크의 선택과 올바른 사용법을 제시하기 위함. 단, 이 권고사항은 지역사회 전파상황에 따라 변경될 수 있음. •적용대상 지역사회 일상생활을 영위하는 개인(단, 의료기관 종사자 등 감염우려가 있는 업무 종사자, 감염자는 제외) •마스크 착용이 필요한 경우와 사용법 1) 보건용 마스크(KF80 이상) 착용이 필요한 경우 · 기침, 재채기, 가래, 콧물, 목아픔 등 호흡기 증상이 있는 경우 · 건강한 사람이 신종코로나 바이러스 감염 의심자를 돌보는 경우 · 의료기관을 방문하는 경우 · 많은 사람을 접촉하여야 하는, 감염과 전파 위험이 높은 직업군에 종사하는 사람 예) 대중교통 운전기사, 판매원, 역무원, 우체국 집배원, 택배기사, 대형건물 관리원 및 고객을 직접 응대하여야 하는 직업종사자 등 2) 마스크 사용법 · 마스크를 착용하기 전에 손을 비누와 물로 씻거나 알코올 손소독제로 닦을 것. · 입과 코를 완전히 가리도록 마스크를 착용한 후, 얼굴과 마스크 사이에 틈이 없는 지 확인할 것. · 마스크를 사용하는 동안 마스크를 만지지 말 것. 마스크를 만졌다면 손을 비누와 물로 씻거나 알코올 손소독제로 닦을 것. •마스크 착용이 필요하지 않은 경우: 혼잡하지 않은 야외, 개별 공간. 코로나 바이러스의 입자가 크기 때문에 야외나 환기가 잘되는 곳이라면 마스크의 중요성이 크지 않다라고 할 수 있음. 다. 자가격리대상자 생활수칙 [9] (질병관리본부 권고, 2020.02.06 기준) •감염 전파 방지를 위해 격리 장소 바깥 외출금지 •독립된 공간에서 혼자 생활하기 1) 방문 닫은 채로 창문을 열어 자주 환기시키고, 식사는 혼자서 하기 2) 가능한 혼자만 사용할 수 있는 화장실과 세면대가 있는 공간 사용하기 *공용 화장실, 세면대를 사용한다면, 사용 후 소독(락스 등 가정용소독제)하고 다른 사람이 사용하도록 함. 3) 진료 등 외출이 불가피할 경우 반드시 관할 보건소에 먼저 연락하기 4) 가족 또는 함께 거주하는 분과 대화 등 접촉하지 않기 · 불가피한 경우, 얼굴을 맞대지 않고 서로 마스크를 쓰고 2m 이상의 거리를 두기 5) 개인용품(개인용 수건, 식기류, 휴대전화 등)으로 사용하기 · 의복 및 침구류는 단독세탁 · 식기류 등은 별도로 분리하여 깨끗이 씻기 전에 다른 사람이 사용하지 않도록 하기 6) 건강수칙 지키기 · 비누로 30초이상 흐르는 물에 손 씻기, 기침 등 호흡기증상이 있을 경우 마스크 착용, 마스크가 없으면 소매로 가려 기침하며 기침, 재채기 후 손 씻거나 손 소독 실시하기 •확진환자와 접촉 후 14일이 경과하는 날까지 아래의 방법으로 자가모니터링 1) 자가모니터링 방법 · 매일 아침, 저녁으로 체온을 측정하고 호흡기증상 등 감염 증상이 나타나는지 스스로 건강상태를 체크 · 보건소에서 하루에 1회 이상 연락드리며, 이때 감염 증상 (발열 37.5 ℃ 이상), 호흡기 증상(기침, 인후통 등), 폐렴)이 있을시 알림 라. 중국발 입국자 및 해외방문자 [10] (질병관리본부 권고, 2020.02.17 기준) •검역감염병 오염지역 (2020.2.12. 기준) 1) 검역감염병 오염지역(또는 오염인근지역)을 감시 기간 내 방문(체류 또는 경유) 한 사람은 입국 시 반드시 「건강상태질문서」를 작성하여 검역관에게 제출해야 합니다. 이를 위반할 경우, 검역법 제12조 및 제39조에 따라 1년 이하의 징역 또는 1천만원 이하의 벌금에 처해질 수 있습니다. •해외 여행자를 위한 코로나바이러스감염증-19 예방 수칙 안내 1) 여행전 준비사항 · 여행 전 국가 감염병 발생정보 확인 · www.해외감염병now.kr 에서 확인 가능 또는 질병관리본부 1339콜센터 전화하기 · 해외여행 전 위생용품(손소독제) 및 개인보호구(마스크) 등 준비 2) 여행 중 주의사항 · 흐르는 물에 비누로 30초 이상 손 씻기 등 개인위생수칙 준수 · 여행 중 가금류 및 야생동물 접촉 금지 · 재래시장 방문 자제하기 · 호흡기 증상(기침, 인후통, 호흡곤란 등)이 있는 사람과 접촉하지 않고 외출 시 마스크 착용 3) 여행 후 주의사항 · 입국 시 검역관에게 건강상태질문서 제출 · 귀가 후 14일 이내 발열과 호흡기 증상(기침, 인후통, 호흡곤란 등) 발생 시 질병관리본부 콜센터 (1339) 신고 · 호흡기 증상이 있을 경우 마스크 착용(외출 시 또는 의료기관 방문 시 반드시 착용) · 흐르는 물에 비누로 30초 이상 손 씻기 등 개인위생수칙 준수 · 의료기관 방문 시 해외여행력을 의료진에게 알리기 3. 치료관리 (2020.03.01 기준) 치료 관리는 지지요법으로 구성됨. 외래 환경에서 충분히 격리가 가능한 경증의 환자 대상으로는 자가격리 치료(재택치료)도 가능함. 가. 홈케어(Home care) [11] •자가격리 치료(재택치료)는 외래 환경에서 충분한 격리가 가능한 경증 감염 환자에게는 적절할 수 있음. •해당 환자들의 관리는 타인에 대한 전파 예방 및 즉각적인 입원이 필요한 임상적 악화 모니터링에 중점을 두어야 함. 나. 입원치료: 비약물 요법 [12] •현재 COVID-19에 대한 표준치료지침이 없기 때문에 해당 질병 관련 증상의 완화와 보조요법으로서 경험적으로 사용하고 있음. 1) 수액 보충 혈역학적으로 불안정한 상태일 때, 임상의의 주관적 판단하에 사용 가능함. 2) 호흡 유지 (산소공급 및 호흡보조) O2 포화도가 미달일 때, 임상의의 주관적 판단하에 사용 가능함. 3) Extra Corporeal Membrane Oxygenation (ECMO) O2 포화도가 미달일 때 및 인공호흡기로 목표하는 산소공급을 맞추지 못할 때, 임상의의 주관적 판단하에 사용 가능함. * ECMO는 체외에서 심장과 폐의 역할을 보조하는 의료 기기로, 공급 산소의 농도와 유량 조절을 통해 적정량의 기체 교환을 이뤄내어 인공적인 이산화탄소 배출과 산소의 공급을 수행하는 의료기기로써 호흡기부전과 호흡산증의 치료로 주로 이용되며 심폐의 기능을 대행하는 역할을 함. [그림 2] ECMO 개요 [13]. 다. 약물요법 COVID-19의 항바이러스 치료를 위해 임상시험 약물도 탐색 중임. 사용 가능한 치료제로는 뉴클레오시드 아날로그의 favipiravir (AVIGAN®), remdesivir 및 galidesivir, 프로테아제 억제제로는 lopinavir/ritonavir (Kaletra®) 등이 있음. 1) 항바이러스제 약물 ● 뉴클레오시드 아날로그: 아데닌 또는 구아닌의 유도체로 RNA의존 RNA 중합효소를 타켓으로 하고 바이러스의 RNA 합성을 저해함. ◯ Remdesivir (임상시험단계) · 뉴클레오시드 아날로그 약물로 C형간염 바이러스 치료제로 개발되었으나 최근 SARS-CoV-2에 대한 in vitro시험에서 바이러스부하의 감소를 나타냄 [14]. · 또 여러 Remdesivir 무작위 임상시험이 중증 COVID-19환자를 대상으로 진행 중임 [15]. · 마지막 사용가능한 치료제로써 사용한 최초 COVID-19 환자 중 한 명의 사례보고서 또한 발표되었음 [16]. 이 환자에서 치료제 투여 11-12일 후 바이러스 부하가 감소하는 추세를 보임. − 부작용: In vitro에서 사람 간세포에서의 독성 가능성 확인됨, In vivo에서는 간독성이 확인되지 않음 [17]. ◯ Favipiravir(AVIGAN®) (승인) − 인플루엔자, 에볼라, 황열 등의 바이러스 감염에 효과적임 [18]. − 부작용: 요산증가, 골수억제(neutrophil 감소), 간독성 (황달, AST/ALT 증가 등), 이상행동(sudden running 등), 아나필락시스 및 쇼크, TENS/SJS, 신독성이 보고됨 ●Protease inhibitors: 코로나 바이러스의 4가지 필수효소생성 억제 ◯ Lopinavir/Ritonavir (Kaletra®) − 동물실험에서 SARS-CoV와 MERS-CoV에 항바이러스성을 보임 − HIV감염의 치료제로 쓰이던 약물로, 해당 약물을 신종코로나 바이러스치료에 사용하여 얻은 긍정적 임상결과는 여러 사례보고서에 발표되었음[1920]. 하지만 더 큰 표본의 무작위대조시험을 통해 그 유효성을 검증해야 한다고 한계를 밝힘. − 바이러스 재생산 활동에 필수요소인 3-chymotrypsin-like protease를 저해한다고 알려짐 − 부작용: 간독성, 내분비계 장애 (혈당증가, 콜레스테롤 수치 증가 등), Disulfiram - papain-like protease의 생산 저해 2) Host-targeted agents ●Pegylated interferon alfa-2a, and -2b : 내재성 항바이러스 반응을 촉진함 3) Nitazoxanide: 설사에 대한 치료제로 승인됨 ● SARS-CoV-2 항바이러스성을 보여줌 [21]. − 부작용(12세이상의 1% 미만 발생): 체신경 및 대사(asthenia, fever, pain, allergic reaction, pelvic pain, back pain, chills, fever, flu-like syndrome), 중추신경계(dizziness, somnolence, insomnia, tremor, hypersthesia), 소화계(vomiting, dyspepsia, anorexia, flatulence, constipation) 등 [22]. 라. 현재 국내 치료지침 [23] · Kaletra (lopinavir/ritonavir) ± interferon · Chloroquine · Hydroxychloroquine · Ribavirin (병용 필수) · Remdesivir 마. [WHO의 잠정적 가이드라인] 신종코로나 바이러스 감염의심 중증 급성 호흡기의 임상적 관리 [24] · Supplemental oxygen therapy · Conservative fluid management · Empiric antimicrobials (sepsis 시 1시간 이내 투여) 4. 코로나19 치료제 관련 임상시험 현황 (2020.03.01 기준) 가. 코로나19 관련 임상 시험 현황 •현재 중국을 비롯한 전 세계에서 코로나19와 관련된 임상시험이 ICTRP(International Clinical Trials Registry Platform)의 2020.03.01 기준 263건 확인되고 있음 [25]. 치료제와 백신에 대해 진행 중이거나 계획된 임상시험이 100건이 넘는 것으로 확인되었음. 하지만 연구실 단위에서 준비하고 있는 것까지 포함하면 더 많은 시험이 추진되고 있는 것으로 보임. 나. 현재 모집 중인 코로나19 치료제 임상시험 •대부분 중국에서 진행되고 있으며, 전통 중국의약품에서부터 최근 대두되는 항바이러스제인 칼레트라®(Lopinavir/Ritonavir), 아비간®(Favipiravir), 클로로퀸(Chloroquine) 등 다양한 약제에 대하여 진행되고 있음. 중국 외 국외에서는 홍콩 및 미국에서 각각 1건의 대상자 모집 중인 임상시험이 확인되었음. 국내에서는 현재 등록된 임상시험은 확인되지 않으나, 일부 제약사들이 신약후보물질 가운데 효과가 있을 것으로 보이는 것을 추려 임상시험을 계획하고 있음. •국내 · 현재 ICTRP 및 ClinicalTrials.gov에 등록된 COVID-19 관련 임상시험은 없음. · 의약품안전나라 임상시험 승인 현황에도 확인되지 않았음. · 기사에서만 확인된 부분 [26]: − 코미팜: 식약처에 개발 중인 바이러스 감염증 치료제 후보물질 ‘파나픽스(Panaphix)’의 임상2/3상에 대한 긴급 임상시험계획 신청했음. − 이뮨메드: 서울대병원에서 이뮨메드가 개발 중인 항바이러스 후보물질 ‘HzVSFv13주’의 치료목적의 사용 승인을 했음. − 셀리버리: 상급종합병원 2곳과 사이토카인 폭풍을 억제하는 신약후보물질(iCP-NI)의 임상실험을 위해 계약함. 5. 코로나19 백신 개발 현황 (2020.03.01 기준) 가. 현재 한국 임상시험 및 신속심사 관련 제도 [27] 1) 임상시험약 치료목적 사용승인제도 운영 : 대체치료제가 없는 환자에게 치료 기회를 제공하기 위한 제도이며 긴급 승인 시 당일 승인, 일반적으로는 7일 내 승인함. 2) 의약품 신속심사 [28] · 생명을 위협하거나 중대한 질병의 치료 분야에서 시급한 의학적 과제를 해결할 의약품의 개발과 심사를 신속하고 원활히 진행하여 환자들에게 최대한 신속한 치료제 제공을 위한 제도. · 치료적 확증 임상시험자료 제출을 조건으로 함. 나. 백신 임상시험 현황
1) SARS-CoV의 성공 사례를 기반으로 COVID-19의 백신 개발에 활용하고자 하고 있음. RBD(receptor binding domain)과 binding ACE2에서 SARSCoV과 COVID-19 사이의 차이가 크기 때문에 SARS-CoV의 백신의 효과는 낮을 것으로 예상됨. 2) 현재 clinicaltrial.gov에서 1상 (Safety and Immunogenicity)을 완료하거나 2상으로 허가받은 임상시험이 없음. 3) 2020.02.11에 진행된 WHO 사무총장의 발표에 따르면 유효성 및 안정성이 확립된 백신 개발 예상기간은 18개월임 [29]. 다. 코로나19 백신 개발 현황 (개발 진행 순) 1) 모더나 (미국) · 협력회사: 미국 국립알레르기전염병연구소(NIAID) · 제품명: mRNA-1273 · 개발단계: Phase I · 기타사항: 3~4월 경에 임상 1상 완료예정 및 4월 경 1상 결과 확인 예상됨. 4월 말쯤 20~25명의 건강한 지원자 대상으로 임상시험 시작으로 두 차례 투여해 면역 반응 확인 후 7~8월에 결과 확인 예상됨. NIAID에서 일반 대중이 사용할 수 있게 될 때까지 앞으로 1년 이상 걸릴 것이라고 함 [30]. 2) Shenzhen Geno-immune Medical Institute (중국) [31] · 제품명: LV-SARS-CoV-2-DC · 개발단계: Phase I/II · 참고사항: Clinicaltrails.gov 에서 나오는 정보 외 뉴스 등 다른 사이트에 관련사항 찾을 수 없음 3) 이노비오 (미국) · 개발단계: 전임상 (백신 개발 완료. 동물실험에 착수 · 작용기전: DNA백신으로 바이러스 유전자를 주입해 면역반응 유도 · 참고사항: 6월에 사람대상 임상시험 후 가을에 임상 발표 예정임. 연말까지 백신 승인 및 투여가능성이 시사됨 [323334]. 4) 클로버 (중국 생명공학기업) · 협력회사: GSK · 개발단계: 전임상 (GSK와 협업하여 후보물질 유효성 평가) · 제품이름: S-트라이머 · 작용기전: Spike glycoprotein 타겟 · 기타사항: 2월 28일 GSK와 연구 협력 체결함. GSK는 항원보강제를 제공해 후보물질의 유효성에 대해 평가를 도울 예정임 [35]. 5) 사노피 · 협력회사: 미국 보건복지부의 생물의약품첨단연구개발국 (BRADA) · 개발단계: 전임상 (백신 후보를 만들 계획) · 기타사항: Emergency use approval를 고려하더라도 시판까지 3~4년 이상 소요 예상됨. 사노피는 예전에 SARS 백신 개발한 제약회사임 [36]. References [1] Guan, Wei-jie, et al. Clinical characteristics of coronavirus disease 2019 in China. N Engl J Med., 2020. doi: 10.1056/NEJMoa2002032. [2] Zhou Peng, et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature. 2020. doi: 10.1038/s41586-020-2012-7. [3] Zumla, Alimuddin, et al. Coronaviruses - drug discovery and therapeutic options. Nat. Rev. Drug Discov. 15, 327–347, 2016. [4] Guangdi Li and Erik De Clercq. Therapeutic options for the 2019 novel coronavirus (2019-nCoV). Nat. Rev. Drug Discov., 2020. [5] Morse, Jared S., et al. Learning from the past: possible urgent prevention and treatment options for severe acute respiratory infections caused by 2019‐nCoV. ChemBioChem. 2020. doi: 10.1002/cbic.202000047. [6] The Novel Coronavirus Pneumonia Emergency Response Epidemiology Team. The Epidemiological Characteristics of an Outbreak of 2019 Novel Coronavirus Diseases (COVID-19), China CDC Weekly, 2(8): 113–122, 2020. [7] 꼭 알아야 할 감염병 예방수칙. 질병관리본부 코로나바이러스감염증-19 웹페이지, 보건복지부, 20 Feb. 2020. http://ncov.mohw.go.kr/shBoardView.do?brdId=3&brdGubun=32&ncvContSeq=520 [8] 코로나19 예방을 위한 마스크 사용 권고사항. 질병관리본부 코로나바이러스감염증-19 웹페이지, 보건복지부. (Accessed on March 1st) http://ncov.mohw.go.kr/shBoardView.do?brdId=2&brdGubun=21&ncvContSeq=239 [9] 자가격리자-자가격리대상자 생활수칙. 질병관리본부 코로나바이러스감염증-19 웹페이지, 중앙사고수습본부 & 중앙방역대책본부, 2020. [10] 중국발 입국자 및 해외방문자. 질병관리본부 코로나바이러스감염증-19 사이트, 중앙방역대책본부. 2020. [11] Home care for patients with suspected novel coronavirus (COVID-19) infection presenting with mild symptoms, and management of their contacts. WHO Interim guidance. (Accessed on Mar 1, 2020) [12] Dale Fisher and David Heymann. Q&A: The novel coronavirus outbreak causing COVID-19. BMC Med, 18(57), 2020. doi: 10.1186/s12916-020-01533-w. [13] ECMO Schema, Jürgen Schaub. https://en.wikipedia.org/wiki/Extracorporeal_membrane_oxygenation#/media/File:Ecmo_schema -1-.jpg [14] Wang, Manli, et al. Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro. Cell Res 2020. [15] Gilead Sciences Statement on the Company’s Ongoing Response to the 2019 Novel Coronavirus (2019-nCoV). 31 Jan. 2020. [16] Holshue, Michelle L, et al. First Case of 2019 Novel Coronavirus in the United States. N Engl J Med. 2020. [17] https://www.who.int/ebola/drc-2018/summaries-of-evidence-experimental- [18] De Clercq, E. New nucleoside analogues for the treatment of hemorrhagic fever virus infections. Chem. Asian J. 14, 3962–3968, 2019. [19] Lim, Jaegyun, et al. Case of the Index Patient Who Caused Tertiary Transmission of Coronavirus Disease 2019 in Korea: the Application of Lopinavir/Ritonavir for the Treatment of COVID-19 Pneumonia Monitored by Quantitative RT-PCR. Journal of Korean Medical Science, 35(6):e79, 2020. [20] Wang, Zhenwei, et al. Clinical characteristics and therapeutic procedure for four cases with 2019 novel coronavirus pneumonia receiving combined Chinese and Western medicine treatment. Bioscience Trends, 2020. [21] Wang, M. et al. Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro. Cell Res. 2020. doi: 10.1038/s41422-020-0282-0. [22] Nitazoxanide. DrugBank, www.drugbank.ca/drugs/DB00507. [23] 요양급여의 적용기준 및 방법에 관한 세부사항 안내. 보건복지부, 21 Feb. 2020. [24] Clinical management of severe acute respiratory infection when novel coronavirus (nCoV) infection is suspected. Interim guidance, WHO, 28 Jan. 2020. [25] International Clinical Trials Registry Platform Search Portal, WHO. (accessed on Mar 1st, 2020) [26] Lee, Keum Y, 제약업계, 코로나 19 치료제 개발 활활. 현대경제신문, 28 Feb. 2020. http://www.finomy.com/news/articleView.html?idxno=75649 [27] 환자 치료 기회 확대와 신약 개발 지원 위한 임상시험 발전 로드맵 마련. 식품의약품안전처. https://www.mfds.go.kr/brd/m_99/view.do?seq=43629. [28] 의약품의 신속심사 적용기준에 대한 가이드라인 마련. 식품의약품안전처, 01 Aug. 2018. [29] Kim, Dayoung, WHO 신종코로나 백신 개발, 18개월 걸려…공식 명칭은 COVID-19. 중앙일보, 12 Feb. 2020. https://news.joins.com/article/23704103 [30] Park, Sangjun, 미국 모더나社 코로나 바이러스 백신 개발 착수. 메디칼타임즈, 25 Feb. 2020. http://www.medicaltimes.com/Users/News/NewsView.html?mode=view&ID=1132183&REFERER=N P [31] “Function and Safety Study of SARS-CoV-2 Synthetic Minigene Vaccines.”, ClinicalTrials.gov. www.clinicaltrials.gov/ct2/show/NCT04276896 [32] Lee, Youngwan, 美·中이 지원하는 우한 코로나 백신 개발자는 한국인…연말이면 접종 가능. 조선일보, 21 Feb. 2020. https://biz.chosun.com/site/data/html_dir/2020/02/21/2020022100286.html [33] Lee, Kwangsoo, 美 나스닥 바이오 기업 이노비오, 코스닥 기술성평가 통과. 이데일리, 27 Feb. 2020. https://www.edaily.co.kr/news/read?newsId=01213606625674784&mediaCodeNo=257&OutLnk Chk=Y [34] U.S. Government Begins Human Testing Of Possible COVID-19 Treatment, Will Start Experimental Vaccine Trials In 6 Weeks. KFF, 26 Feb. 2020. [35] Jeon, Yoonmi, 클로버-GSK, 코로나19 백신 후보물질 개발에 협력. 청년의사, 28 Feb. 2020. https://www.docdocdoc.co.kr/news/articleView.html?idxno=1077873 [36] Branswell, Helen. Sanofi announces it will work with HHS to develop coronavirus vaccine. STAT, 18 Feb. 2020. |