동향분석
Home > 뉴스브리핑센터 > 동향분석| [NRF 동향] 혈류 감지하는 세포 안테나, 섬모에 의한 혈관생성기전 규명! |
|
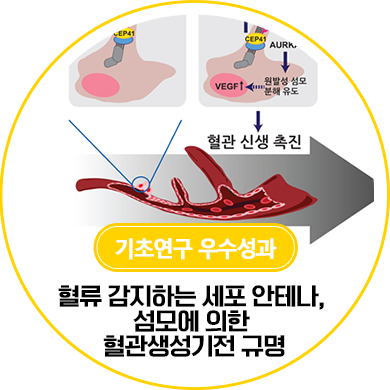
혈류 감지하는 세포 안테나, 섬모에 의한 혈관생성기전 규명 제브라피쉬에서 환경변화에 따른 섬모 분해와 그에 따른 혈관신생 기전 규명 세포 밖 상황을 감지하여 세포 안의 변화를 이끌어 내는 세포의 안테나, 원발성 섬모. 거의 모든 세포에 존재하지만, 대사질환이나 신경 발생 질환과의 연관성에 한정되어 연구가 이뤄지고 있습니다. 그 가운데 혈관신생 과정에서의 원발성 섬모의 역할에 대한 연구결과가 나왔습니다. 이지은 교수(성균관대학교) 연구팀이 혈관내피세포 밖으로 돌출된 원발성 섬모의 혈관신생 과정에서의 역할과 분자적 기전을 규명했다는 소식입니다! 종양의 증식과 전이 시 혈관신생이 두드러지게 나타나는 만큼, 원발성 섬모를 표적으로 하는 항암제 개발 연구의 단초가 될 것으로 기대되고 있습니다. 연구팀은 유전자 가위로 섬모 조절 유전자, CEP41을 없앤 돌연변이 제브라피쉬에서 혈관 직경 감소와 이상 혈관 생성 등을 관찰하고, 원발성 섬모와 혈관신생의 연결고리를 찾아냈는데요. *혈관신생(angiogenesis) : 기존 혈관으로부터 새로운 혈관이 생성되는 현상. 내피세포의 침투나 이동, 증식, 분화 등의 과정을 거쳐 산소와 영양분을 공급하기 위한 필수적인 과정 *제브라피쉬(Zebrafish) : 잉엇과의 얼룩무늬 열대어로 관찰이 쉽고 빠른 배아 발달 및 거의 완벽한 게놈 분석으로 바이오의료연구에 널리 사용되는 대표 동물모델 CEP41 단백질이 원발성 섬모를 구성하는 튜블린 단백질을 변형 (글루타밀화)시키면, 이것이 신호가 되어 섬모 분해와 혈관 생성 인자 생성을 촉발, 결국 혈관신생으로 이어지는 일련의 과정을 밝혀낸 것입니다.
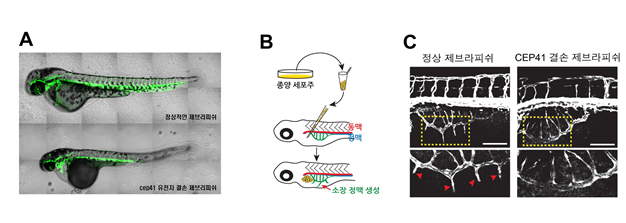
섬모 조절 유전자 CEP41이 결손된 제브라피쉬에서 나타난 혈관 형성 이상 CEP41은 대표적 원발성 섬모 질환군의 하나인 주버트 신드롬의 원인 유전자로, 신경 발생 과정에서의 역할만 알려져 있었습니다. 실제 CEP41 유전자가 결손된 돌연변이 제브라피쉬에 많은 산소와 영양분을 소비하는 종양 세포주를 이식하더라도 소장 정맥 생성 등의 혈관신생이 잘 이뤄지지 않았는데요.
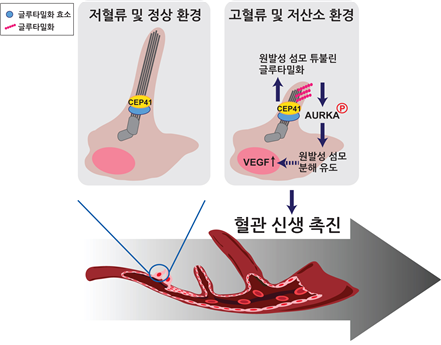
CEP41에 의한 혈관내피세포 섬모 분해를 통한 혈관신생 조절 기전 이 같은 혈관신생 이상은 동물모델에서뿐만 아니라 인간 혈관 유래 세포에서도 관찰되었습니다. CEP41 유전자 발현이 줄어든 세포는 이동성과 침습능, 상처치유능, 혈관생성능도 절반 가까이 감소했습니다. 혈류 이상이나 조직 손상에 따른 심혈관계 질환이나 무분별한 세포증식에 따른 과다한 산소 소비로 저산소 상황에 놓이는 종양에서 이번에 규명된 혈관신생에 관여하는 분자들(CEP41, AURKA) 및 원발성 섬모를 표적으로 하는 치료제 개발 연구의 실마리가 될 것으로 기대됩니다. 이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 X-project, 중견 연구(보호 육성), 기초연구실(BRL) 사업의 지원으로 수행되었으며, ‘엠보 리포츠(EMBO Reports)’에 2019년 12월 29일 게재되었습니다.
|