동향분석
Home > 뉴스브리핑센터 > 동향분석| [NIKOM 동향] ‘2019년 의약품 허가 보고서’ 발간 |
|
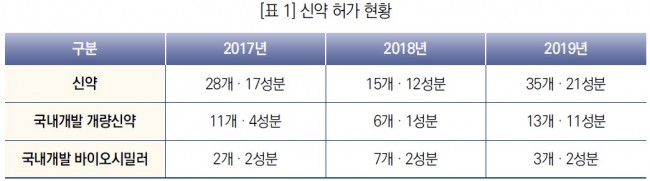
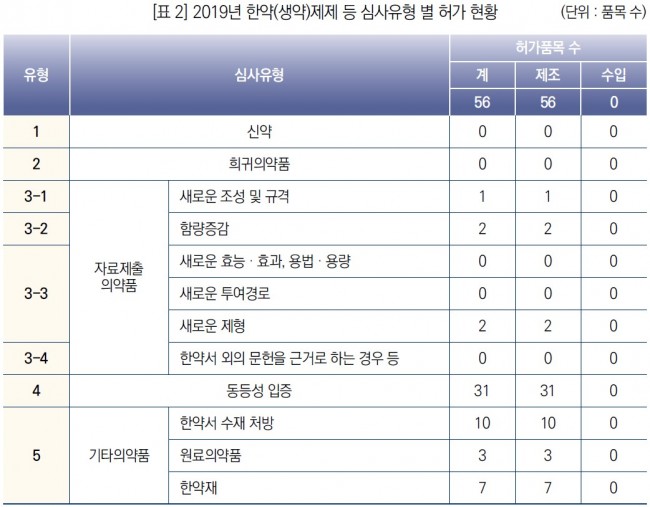
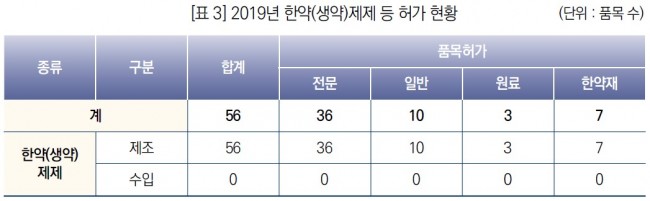
» 식품의약품안전처는 4월 28일 지난해 의약품 허가 · 신고 현황을 담은 ‘2019년 의약품 허가 보고서’ 발간 • 지난해 의약품 허가 · 신고 현황의 주요 특징은, - (새로운 제형 형태의 제품개발 증가) 새로운 제형(71개 품목, 38.8%)의 국내 개발이 두드러졌으며, 기존의 ‘캡슐제’를 정제 등 다른 ‘경구용 제제’로 개발하거나 ‘현탁용 분말’을 ‘산제’로 개발한 경우와 ‘일반(속방성) 제제’를 약의 복용 횟수를 줄여 편의성을 높인 ‘서방성 제제*’로 개발한 경우가 강세 * ‘일반(속방성) 제제 : 유효성분의 방출 속도를 따로 조절하지 않는 제제 서방성 제제 : 투여 횟수를 줄이기 위해 특수한 가공을 통해 일반적으로 일반(속방성) 제제에 비해 유효성분이 천천히 방출되도록 만든 제제 - (국내 개발 개량신약 및 바이오시밀러 개발 상승 추세) 신약 35개 품목이 허가되었으며, 이 중 국내 신약은 4개 품목, 수입 신약은 31개 품목. 제품 특성별로는 화학의약품 28개 품목, 생물의약품 7개 품목임. 신약 허가는 전년 대비 증가하였고, 국내 개발 개량신약과 바이오시밀러도 꾸준히 개발
- (신경계 용의약품 강세) 약효군별 분류에 따르면 해열 · 진통 · 소염제 등이 포함된 ‘신경계용 의약품’이 1,070개 품목(22.2%)으로 가장 많이 허가
참고: 식품의약품안전처, 「2019년 의약품 허가 보고서」 발간, 2020.04.28. 출처: NIKOM 한의약 동향 브리프 |